A természettudósok a
vizet sokáig az egyszerű anyagok közé sorolták. Szerkezeti felépítését csak a
XVIII. sz második felében sikerült tisztázni. Henry Cavendish angol kémikus
megfigyelte, hogy hidrogén (ezt akkoriban gyúlékony levegőnek hívták) és
levegő (akkoriban közönséges levegő) robbantásakor a hidrogén és a
levegő 1/5-e egyesül (a levegő 21%-a oxigén) és páraként csapódik le. Tehát a
pára hidrogénből és oxigénből áll. Cavendish a későbbiekben a térfogati
viszonyokat is vizsgálta, s azt kapta, hogy két egység hidrogénből és egy egység
oxigénből keletkezik a víz. Kísérleteit a francia származású Antoine
Lavoisier (Lavoisier korábbi
tanulmányodban) összegezte, illetve következtetett a végső megoldásra. Lavoisier
1783-ban bejelentette, hogy a víz két egység hidrogénből és egy egység oxigénből
áll.
A természettudósok a
vizet sokáig az egyszerű anyagok közé sorolták. Szerkezeti felépítését csak a
XVIII. sz második felében sikerült tisztázni. Henry Cavendish angol kémikus
megfigyelte, hogy hidrogén (ezt akkoriban gyúlékony levegőnek hívták) és
levegő (akkoriban közönséges levegő) robbantásakor a hidrogén és a
levegő 1/5-e egyesül (a levegő 21%-a oxigén) és páraként csapódik le. Tehát a
pára hidrogénből és oxigénből áll. Cavendish a későbbiekben a térfogati
viszonyokat is vizsgálta, s azt kapta, hogy két egység hidrogénből és egy egység
oxigénből keletkezik a víz. Kísérleteit a francia származású Antoine
Lavoisier (Lavoisier korábbi
tanulmányodban) összegezte, illetve következtetett a végső megoldásra. Lavoisier
1783-ban bejelentette, hogy a víz két egység hidrogénből és egy egység oxigénből
áll.
A vízmolekulában a hidrogéneket és az oxigént kémiai kötés kapcsolja össze. A vízben előforduló kémiai kötést kovalens kötésnek nevezzük. A kovalens kötés kötőelektronpárokkal jön létre.
| Rajzold le a hidrogénatomot, jelölve a legkülső elektront! | Rajzold le az oxigénatomot, jelölve a legkülső elektronokat! | Rajzold le a vízmolekula szerkezeti képletét, jelölve a nemkötő elkektronpárokat! |
|
hidrogénmolekula |
oxigénmolekula |
|
Az oxigén és a hidrogén eltérő elektronnegatívitásából következik, hogy az oxigén jobban maga felé vonzza a kötőelektronokat, így polaritás alakul ki. Ennek köszönhetően a vízmolekulában poláris kovalens kötés van. Poláris tulajdonsága miatt a víz a leggyakrabban használt oldószer.
Vajon mivel magyarázhatók a vízmolekula szinte egyedüálló tulajdonságai? Magas olvadás- és forráspont, magas hőkapacitás stb.
 A poláris kötésekben levő H atomok (amelyek
részlegesen pozitív töltésűek) és egy szomszédos vízmolekula (negatív töltésű)
nemkötő elektronpárja között vonzóerő alakul ki. Ez a molekulák közötti
kölcsönhatás egy másodrendű kötés kialakulásához vezet, amit hidrogénkötésnek
nevezünk. A hidrogénkötés kialakulásának feltétele, hogy a H-hez nagy
elektronegativitású atom (pl. N, O, F) kapcsolódjék. A vízmolekulák között
kialakuló hidrogénhíd a legerősebb az intermolekuláris (molekulák közötti)
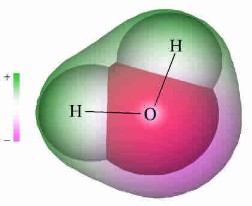
kölcsönhatások közül. A képen a vízmolekulán belüli töltéseloszlás
látható. Lila színnel a negatívabb, zöld színnel a kevésbé negatívabb területek.
A poláris kötésekben levő H atomok (amelyek
részlegesen pozitív töltésűek) és egy szomszédos vízmolekula (negatív töltésű)
nemkötő elektronpárja között vonzóerő alakul ki. Ez a molekulák közötti
kölcsönhatás egy másodrendű kötés kialakulásához vezet, amit hidrogénkötésnek
nevezünk. A hidrogénkötés kialakulásának feltétele, hogy a H-hez nagy
elektronegativitású atom (pl. N, O, F) kapcsolódjék. A vízmolekulák között
kialakuló hidrogénhíd a legerősebb az intermolekuláris (molekulák közötti)
kölcsönhatások közül. A képen a vízmolekulán belüli töltéseloszlás
látható. Lila színnel a negatívabb, zöld színnel a kevésbé negatívabb területek.
Hidrogénkötés kialakulása - animáció
Még egy különleges tulajdonság
Amikor a víz
megfagy, a hidrogénkötések főszereplésével egy tetraéderes szerkezet alakul ki,
amelyben a térkihasználás elég rossz, így nagy hézagok, üregek vannak benne. Ez
okozza azt, hogy a jég sűrűsége kisebb, mint a vízé és fagyáskor a többi
anyagtól eltérően a víz térfogata megnő (mintegy 9%-kal).
A jég 9 féle módosulatban kristályosodik ki.